ヒト幹細胞培養(高濃度ヒト幹細胞培養ドライフリーズ)ドライフリーズとは?
1、AT高濃度ヒト幹細胞(100 HMSC-AT)脂肪組織間葉系幹細胞骨髄や脂肪組織などに存在する間葉系幹細胞は、新しい細胞の“種子”を増加させる細胞となりうる。身体修復や再生を行う幹細胞は加齢とともに減少する。幹細胞が減少すると,組織の修復には老化が間に合わなくなる。この減少した幹細胞を補充することで,傷ついた部分や老化した部分を修復し,身体全体を若返らせる。
脂肪幹細胞には“自己複製能力”と“分化能力”の2つの特性がある。同様の特性を有する成体幹細胞としては,他に臍帯血,胎盤,骨髄,特に脂肪幹細胞があり,採取が容易であり,大量の幹細胞を採取できることが注目されている。
培養した脂肪由来の間葉系幹細胞を体内から取り出すと,増殖因子の分泌が活発になる。体内に戻ると,骨細胞,軟骨細胞,線維芽細胞,骨格筋細胞,脂肪細胞などに分化し,分泌される増殖因子は他の細胞の成長にも良い影響を与える。

2.AT高濃度ヒト幹細胞(100 HMSC-AT)
高濃度ヒト幹細胞培養ドライフリーズ、抗衰老不仅是女人的事!男のアンチエイジングも見逃せない!幹細胞の抗老化は筋体内の素力を通じて内から外へ生体機能を発揮し、老化細胞の世代交代を正常にし、それによって抗老化の目的を達成することができる。初めて幹細胞(100 HMSC-AT)を使用することは明らかに身体の各システム機能の総合的な改善を感じ、即ち美容抗老化、睡眠を助けることができ、また潜在疾病を予防することができ、未然に防止することができる。体細胞の更新速度を高め、人体はエネルギーと活力に満ちており、自然とますます若くなり、老化や長寿を遅らせる目的を根本的に達成しています!AT高濃度ヒト幹細胞、青春のガソリンスタンド

3、AT高濃度ヒト幹細胞(100 HMSC-AT)はヒト脂肪組織間葉系幹細胞由来であり、ヒト内に存在する歯髄、臍帯、骨髄、脂肪など間葉系幹細胞に分類される幹細胞を培養し、細胞数を増加させる際に二次的に発生する溶液は“ヒト由来幹細胞培養上清”と呼ばれる。
幹細胞培養液から幹細胞を取り出した後,種々の滅菌処理を行った液体(上清)というヒト幹細胞培養上清には幹細胞と同様の細胞伝達剤が含まれており,幹細胞と同様の効果が観察され,臨床医学的使用が開始された。効果についても確認された。AT高濃度人体幹細胞効果:1、アンチエイジング、皮膚が滑らかになり、潤い、肌の色が白くなり、細かいしわが浅くなり、顔のシミが薄くなり、全身の皮膚が引き締まって、乳房の膨らみがきつくなって弾力がある2、免疫力を高め、睡眠を改善し、疲れにくい、エネルギッシュ3、血液循環を促進し、抗酸化、女性更年期症状を緩和する4、人体機能を全面的に向上させ、体内ホルモンレベルを調節する、新陳代謝を高める5、病気の予防、抗ウイルス、炎症を抑制し、創傷面の癒合を加速!

4、100 HMSC-AT(高濃度ヒト幹細胞培養ドライフリ-ズ)はヒト脂肪組織間葉系幹細胞から由来し、幹細胞を利用して体内の他の細胞に分化し、各種の退行性、壊死性、侵襲性、代謝と退行性病変を再生と再固定し、罹患或いは退化した組織と器官構造を回復し、そしてこの独特な機能を持つ。各種の老化した、損傷した組織細胞を修復、交換し、筋肉基礎細胞の起源を修復し、細胞に若い生理能力を回復させ、細胞に持続的な青春活力を持たせ、そして内から外へ色落ち汚れ、細紋を平らにし、肌に柔軟感を回復させ、引き締めを回復させ、美白と白色肌を明るくする。幹細胞美容抗老化は、医学的角度から見ると、抗老化は全体、統合、深さの医学行為であり、顔面だけでなく、全方位、立体、深層抗老化のみであり、内から外まで最適な抗老化効果を実現し、身体を活力に満ち、免疫力を高め、顔の問題を改善する。

5.AT高濃度ヒト幹細胞(100 HMSC-AT)は、皮膚再生医療においてコラーゲン、ヒアルロン酸、エラスチンなどが存在する。いずれも弾性,潤い,弾性などの基本要素であり,これらは皮膚細胞から作られており,若さを保つために働いている。
普段の生活では、皮膚細胞はストレスや紫外線などでダメージを受ける。また,加齢とともに皮膚の機能も衰え,数も減少する。皮膚細胞が衰退すると,皮膚に必要な要素も生じず,しわやたるみなどの原因となる。このような傷害を受けた皮膚に“線維芽細胞”,“PRP”などを移植することで,衰弱した皮膚組織を修復する役割を果たす。その結果,コラーゲン,ヒアルロン酸,エラスチンなどが再生成し,皮膚組織が改善した。肌自体が元の若さに戻る。ヒアルロン酸などの異物を注入する治療とは異なり,体内に吸収されることなく,長期的に老化速度を遅らせることができる。

6.100 HMSC-AT高濃度ヒト幹細胞培養液を心から推薦する:幹細胞は医学界の“万能細胞”と呼ばれている。炎症とアレルギーを抑制し、粗い肌を改善し、ニキビあとを薄め、美白してシミを除去し、しわと皮膚の弾性を改善し、内分泌を調節し、老化細胞を修復することができる。根本的に老化を遅らせる、逆齢効果を達成!適用者:1.老化、皮膚のくすみ、たるみ、顔面美容2を予防する。内分泌及び性機能低下者3。免疫力低下、全身痛などの症状者4。睡眠不足、情緒不良、身体機能退化5。新陳代謝が遅く、月経失調など6。病気や抗ウイルスなどを予防し、月に1回(効果が最適になる)細胞再生を活性化し、コラーゲン生成を促進し、皮膚の光沢や弾力を増加させることをお勧めします!AT高濃度人体幹細胞は、日本銀座のハイエンド医療アンチエイジング製品から出て、細胞栄養因子を分泌することによって、健康細胞に対する栄養と修復を実現し、それによって人体に対する全面的な修復を実現する。AT高濃度人体幹細胞は、筋肉のすべての細胞、一寸の肌、すべての器官、一秒ごとの精神を青春活力に満ちさせる。私たちを持続させる:健康、青春、そして美しい!

幹細胞治療(自己脂肪由来)とは?
幹細胞とは?
わたしたちはみな、自分たちのからだのなかに、皮膚や血液のように、ひとつひとつの細胞の寿命が短く、絶えず入れ替わり続ける組織を保つために、失われた細胞を再び生み出して補充する能力を持った細胞を持っています。こうした能力を持つ細胞が「幹細胞」です。幹細胞と呼ばれるには、次の二つの能力が不可欠です。一つは、皮膚、赤血球、血小板など、わたしたちのからだをつくるさまざまな細胞を作り出す能力(分化能)、もう一つは自分とまったく同じ能力を持った細胞に分裂することができるという能力(自己複製能)です。
幹細胞は大きく2種類に分けられます。一つは、皮膚や血液のように、きまった組織や臓器で、消えた細胞のかわりを造り続けている幹細胞です。このタイプの幹細胞は「組織幹細胞」と呼ばれています。組織幹細胞は何にでもなれるのではなく、血をつくる造血幹細胞であれば血液系の細胞、神経系をつくる神経幹細胞であれば神経系の細胞のみ、というように、役目が決まっています。もう一つは、ES細胞(胚性幹細胞)のように、わたしたちのからだの細胞であれば、どのような細胞でも作り出すことのできる「多能性幹細胞」(Pluripotent Stem Cell)です。つまり、多能性幹細胞は、わたしたちのからだのなかにある様々な組織幹細胞も作り出すことができるのです。iPS細胞(induced Pluripotent Stem Cell)とは、普通の細胞をもとにして人工的につくった「多能性幹細胞」のことなのです。
こうした「幹細胞」の性質を利用して、細胞そのものを薬として怪我や病気を治す「再生医療」という新しい治療法の研究や、体内の細胞の状態をからだの外で再現して病気のしくみを調べる研究が進んでいます。
MSC(間葉系幹細胞)の原理
糖尿病性心筋症に対するMSC移植の効果。(a)MSCはMMP-2の活性化を増大させ、MMP-9の活性化を抑制し、心臓のリモデリングを減弱させる。(b)MSCはVEGF、IGF-1、AM、HGFを生成し、損傷した心筋における筋形成および血管新生を刺激する。(c)心筋細胞および血管内皮細胞への分化を介して、MSCは心筋灌流および心筋再生を改善する。略語:AM、アドレノメデュリン; HGF、肝細胞増殖因子; IGF-1、インスリン様成長因子-1; MMP、マトリックスメタロプロテアーゼ; MSC、間葉系幹細胞; VEGF、血管内皮成長因子

間葉系幹細胞の全身投与は、細胞媒介作用を含む末端(内分泌)または局所(パラクリン)効果を誘発することができる。1) 血管内皮成長因子(VEGF)、インスリン様成長因子1(IGF-1)、単球化学誘引物質タンパク質1(MCP1)、塩基性線維芽細胞増殖因子(bFGF)、インターロイキン6(IL6) 2) 幹細胞増殖および分化: 幹細胞因子(SCF)、白血病阻害因子(LIF)、マクロファージコロニー刺激因子(M CSF)、ストロマ細胞由来因子1(SDF1)、アンギオポイエチン1、アクチビンA 3) 線維症の阻害:肝細胞成長因子(HGF)、bFGF、アドレノメデュリン(ADM) 4) アポトーシスの阻害:VEGF、HGF、IGF1、形質転換成長因子(TGF)β、bFGF、顆粒球マクロファージコロニー刺激因子(GM CSF)、アクチビンA、トロンボスポンジン1。免疫介在作用には以下のものが含まれる(5〜8) 5) TおよびB細胞の抑制:ヒト白血球抗原G5(HLA G5)、HGF、誘導性一酸化窒素合成酵素(iNOS)、インドールアミン2,3ジオキシゲナーゼ(IDO)、プロスタグランジンE2(PGE 2)、bFGF、TGFβ 6) 制御性T細胞(Treg)のTGFβ発現による分化および増殖の誘導。 7) IDO、PGE 2およびTGFβの分泌によるナチュラルキラー(NK)細胞の阻害。 8) PGE 2の分泌による樹状細胞(DC)成熟の阻害。
図「Stem Cell Res Ther」はCarriónとFigueroaにより再現された。2011年5月11日;2(3):23.
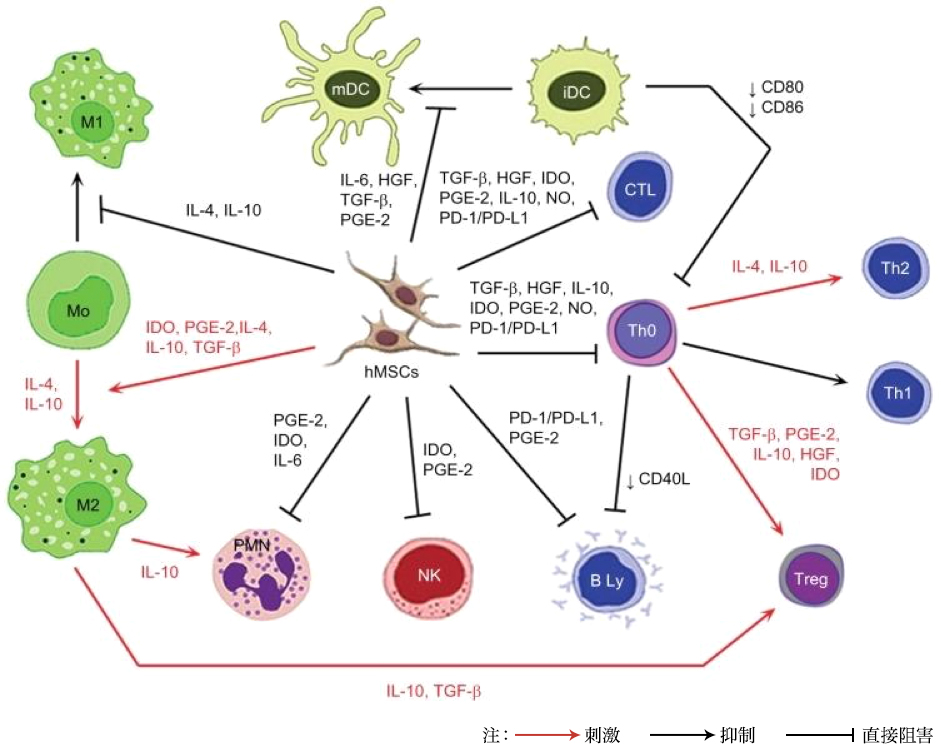
注:赤い矢印:刺激;黒い矢印:抑制;鉤のない矢印:直接阻害
略語:iDC、未成熟樹状細胞; IL、インターロイキン; HGF、肝細胞増殖因子; TGF-β、形質転換成長因子-β; PGE-2、プロスタグランジンE2; IDO、インドールアミン2,3-ジオキシゲナーゼ; NO、一酸化窒素; PD-L1、プログラムされた死リガンド1; hMSC、ヒト間葉系幹細胞; Treg、T regulatory; Th、Tヘルパー; CTL、細胞傷害性T細胞; mDC、成熟樹状細胞; PD-1、プログラム細胞死タンパク質1; PMN、多形核白血球; NK、NK細胞
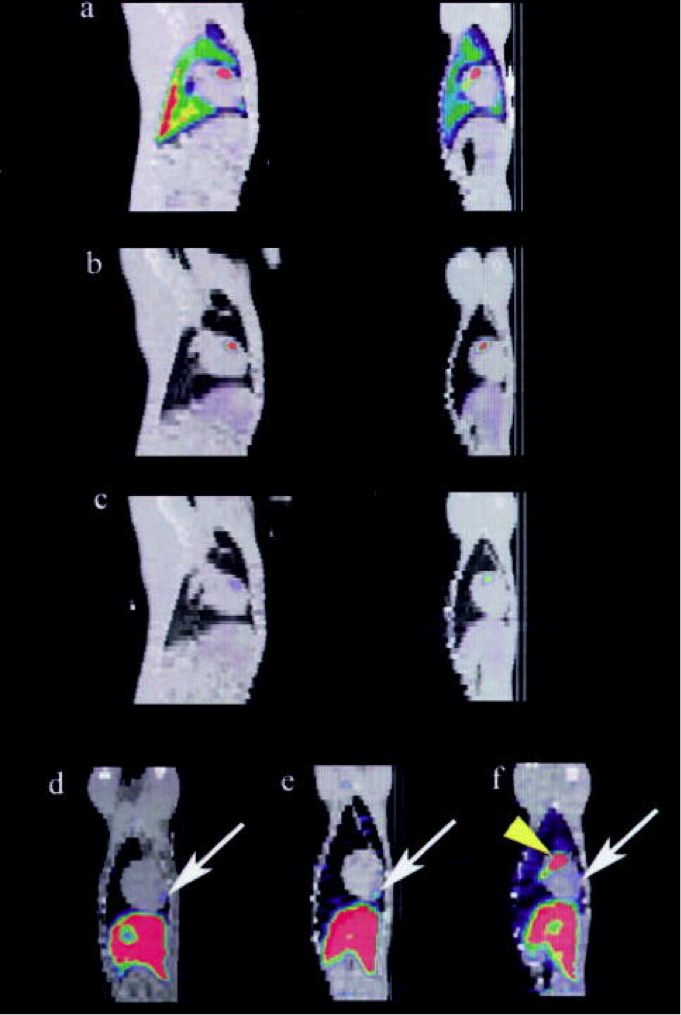
動物の心臓の前脳室領域における局所的取り込みを示した1日目(a)、2日目(b)および7日目(c)に融合したSPECT / CT画像の矢状面(左)および冠状面(右)の図である。最後の撮影時点(5〜8日目)では、MSC摂取の前頂部領域(矢印)は、冠状構造図において3つの代表的な動物に示されている。 これより前方の頂点分布は、初期焦点ホットスポットが観察されたかどうかに関係なく存在した。(fの黄色の矢印のみ)
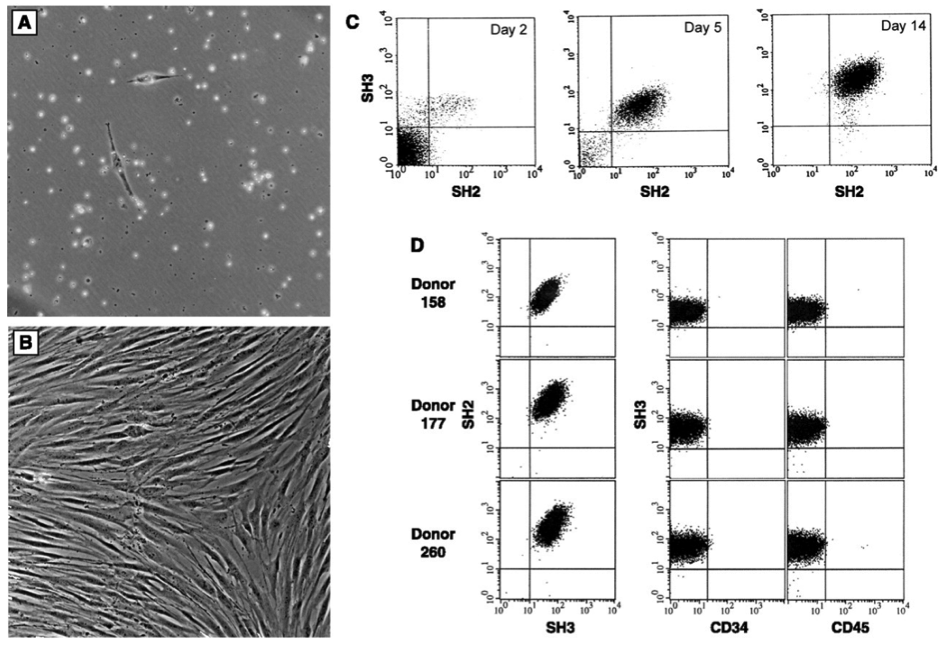
単離骨髄間質細胞の特徴。細胞は密度分画後に骨髄から培養され、プレーティングの48時間後が(A)、プレーティングの10日後が(B)として示されている。(C)流動細胞計測法は、培養されたこれらの細胞の濃縮を示す。結果は表面マーカーに対して生じた抗体SH2およびSH3を用いて、培養の2日目、5日目、および14日目に得られた。(11)14日目、細胞は95〜99%均質であり、造血系の細胞に共通する抗原CD14、CD34(Becton-Dickinson)、またはCD45(Pharmingen)に対する反応が陰性であった。(D)単離手順の均質性および再現性は、流動細胞計測法によって実証された。
MSC(間葉系幹細胞)の原理
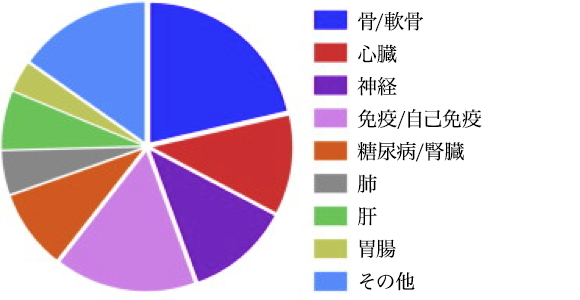
臨床試験でのMSCを用いて適応される適応症。 352の登録された臨床試験のデータ
Indications Being Addressed using MSCs in Clinical Trials. Data for 352 registered clinical trials.
Citation// Stem Cell Therapies in Clinical Trials: Progress and Challenges. Trounson, Alan et al. Cell Stem Cell , Volume 17 , Issue 1 , 11 – 22
疾患別・加齢による疾患
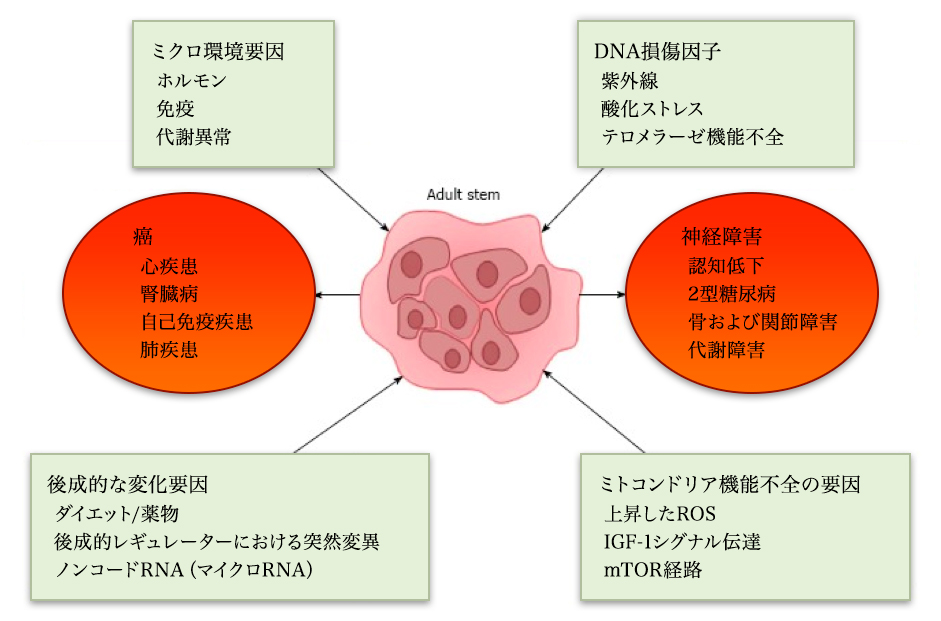
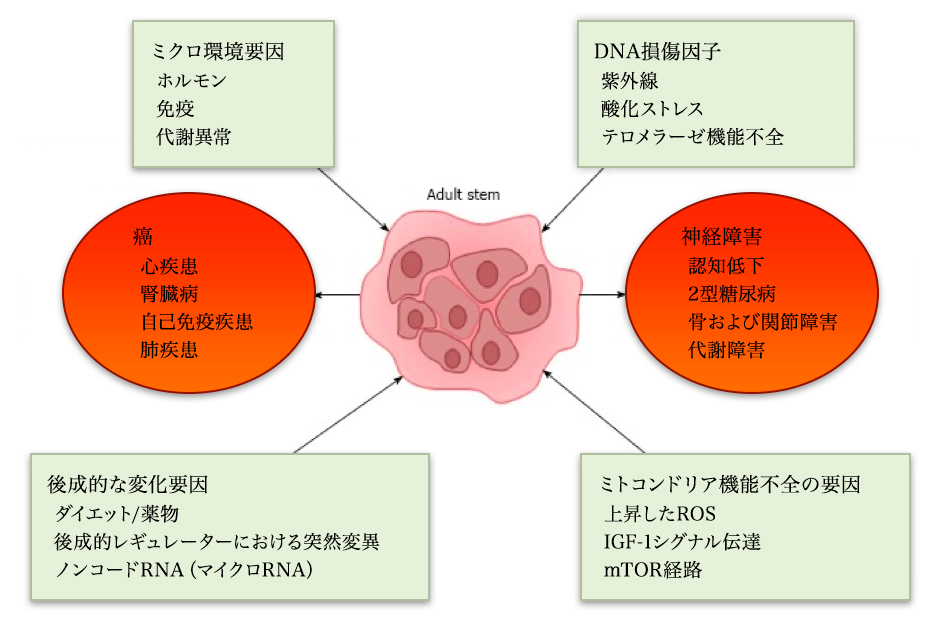
多能性幹細胞は顕著な自己再生能を有し、複数の多様な細胞に分化することができる。老化プロセスが幹細胞に悪影響を及ぼす可能性があるという証拠が徐々に増えている。幹細胞が老化すると、その再生能力が低下し、様々な細胞型に分化する能力が変化する。 したがって、老化に起因する幹細胞機能の低下が、様々な老化関連疾患の病態生理において重要な役割を果たす可能性が示唆されている。老化関連疾患の病態生理を理解するだけでなく、将来の老化関連疾患を治療するための有効な幹細胞ベースの治療法の開発においても、幹細胞機能の老化プロセスの役割を理解することは重要である。このレビュー記事は、さまざまな老化関連疾患連幹細胞機能不全の基礎に焦点を当てている。次に、老化関連幹細胞機能不全の原因となる可能性のあるメカニズムに関するいくつかの概念について述べる。また、開発中である老化に関連する幹細胞欠損のための現在の潜在的な治療法について簡単に議論する。
Citation// World J Exp Med. 2017 Feb 20; 7(1): 1–10.Effect of aging on stem cells. Abu Shufian Ishtiaq Ahmed,et al
疾患別・肝臓/糖尿
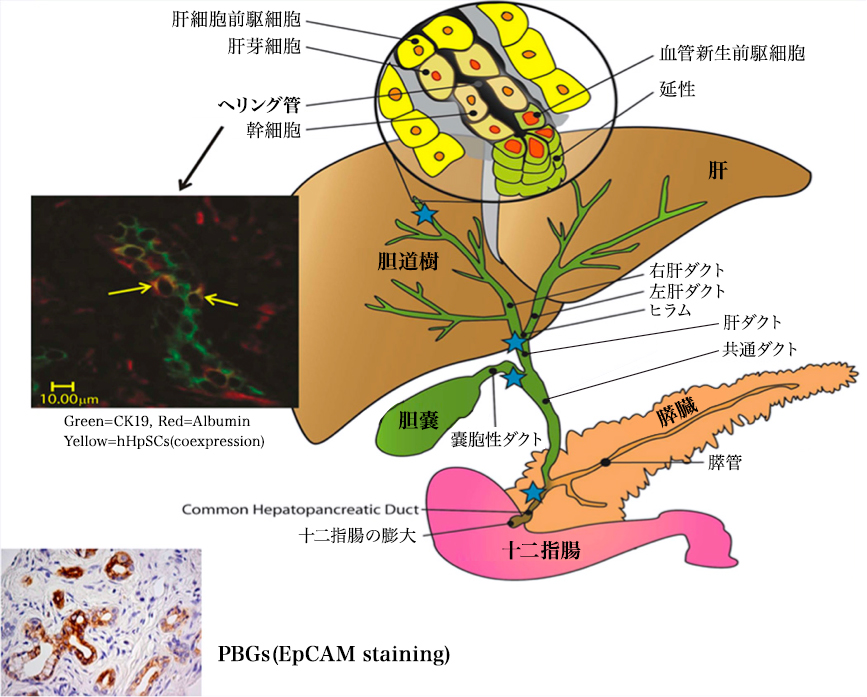
再生医療は、損傷した臓器の修復のために幹細胞/前駆細胞療法を用いて臨床プログラムに移行している。肝臓および膵臓、内胚葉系幹細胞集団を共有する器官、胆道幹に位置する胆道系幹細胞(hBTSC)について手短に述べる。それらはヘリング管内の肝幹/前駆細胞の前駆体であり、膵管腺の前駆細胞である。それらは、胆管壁内の半径方向軸に沿った成熟系統、および十二指腸を始点とし、肝臓または膵臓中の成熟細胞で終わる近位
– 遠位軸を生じる。種々の肝疾患患者の肝動脈に移植された幹細胞(胎児肝臓由来の肝幹/前駆細胞)の影響を評価する臨床試験が、長年にわたって行われてきた。免疫抑制は必要ではなかった。所与の基準を与えられた対照被験者はすべて、1年以内に死亡したか、または肝機能が低下した。100〜150百万個の肝臓幹/前駆細胞を移植した被験者は、肝機能および数年にわたる生存期間の改善を示した。移植の安全性と有効性の評価はまだ発展途上である。hBTSCを用いた糖尿病のための幹細胞療法は、まだ研究されているが、進行中の前臨床試験の後に行われる可能性が高い。さらに間葉系幹細胞(MSC)および造血幹細胞(HSC)は、慢性肝疾患または糖尿病の患者に使用されている。MSCは、栄養因子および免疫調節因子の傍分泌を介して効果を示しており、成熟実質細胞または膵島細胞への非効率な系統制限は限られている。
HSCの効果は、主に免疫機構の調節によるものである。
Stem Cells. 2013 Oct;31(10):2047-60. doi: 10.1002/stem.1457. Concise review: clinical programs of stem cell therapies for liver and pancreas.Lanzoni G1, Oikawa T
糖尿病
QinanWu, Bing Chen, and Ziwen Liang,
Mesenchymal Stem Cells as a Prospective Therapy for the Diabetic Foot
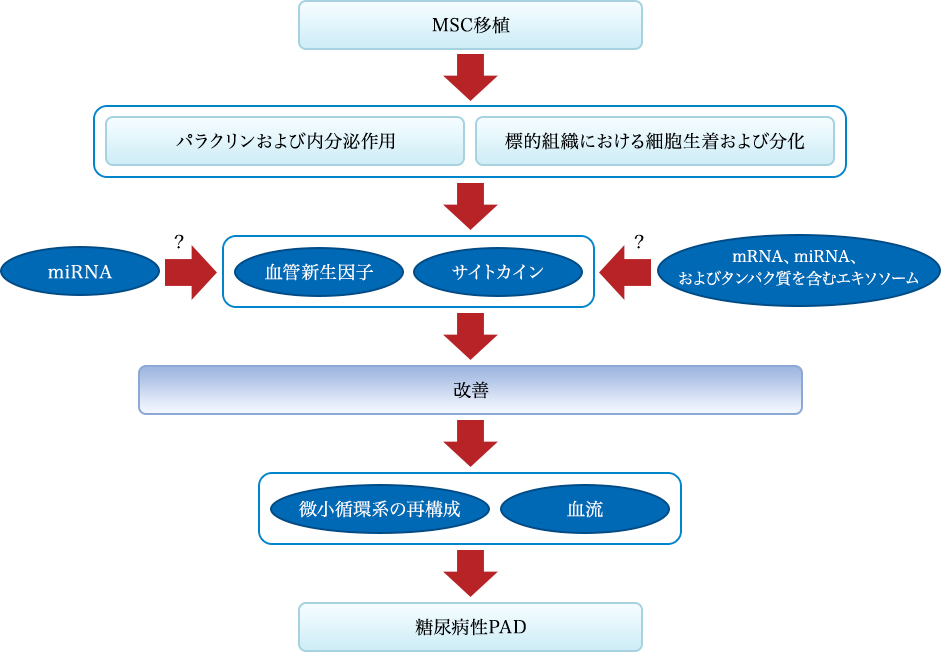
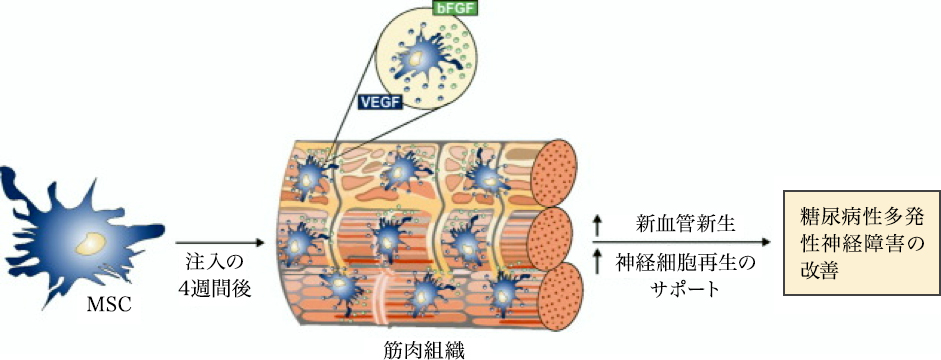
図1:糖尿病性PADに対するMSCの移植の効果のメカニズム。2つの経路からの幹細胞移植によって媒介される回復効果のメカニズム:1つは血管新生因子およびサイトカインの分泌であり、もう1つは細胞の組織構成成分への移植および分化である。幹細胞は、血管新生因子およびサイトカインの局所分泌および発現を特異的に改善することができ、微小循環系の再構築および血流および膵島β細胞機能の改善に寄与し、糖尿病性PADの改善につながる。幹細胞は、内皮細胞の機能不全の回復を達成するために内皮細胞に分化することもできる。これらの影響は、miRNAおよびMEXに関連する可能性がある
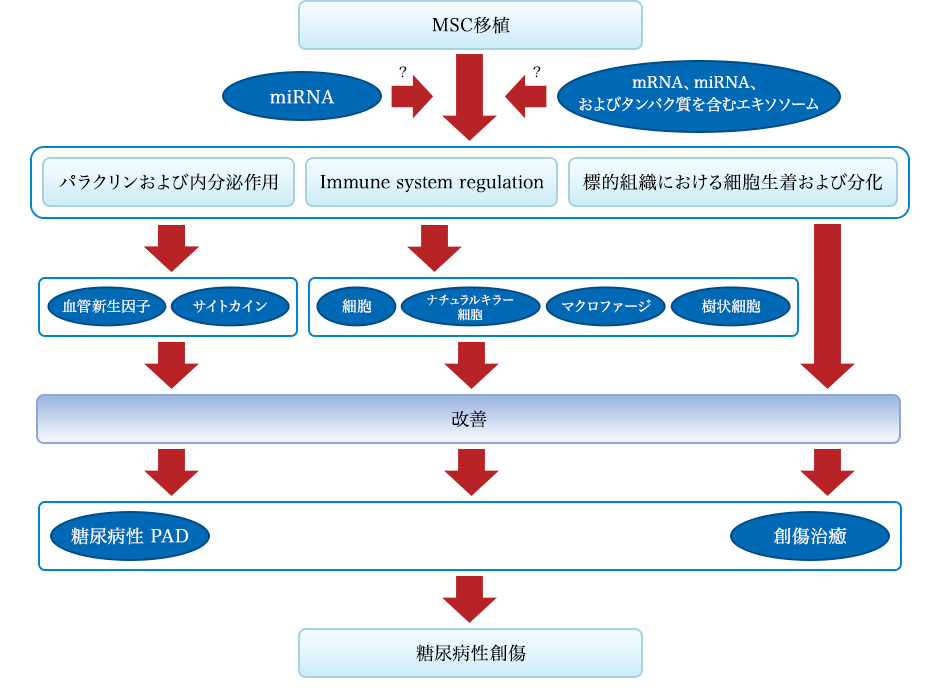
図2:糖尿病性創傷へのMSC移植の効果のメカニズム。3つの経路からのMSC移植による糖尿病創傷回復:第1は血管新生および因子およびサイトカインの分泌であり、第2は免疫系の調節であり、第3は細胞の組織構成成分への移植および分化である。幹細胞は、糖尿病性PADおよび糖尿病の改善に寄与する血管新生因子およびサイトカインの局所分泌および発現を特異的に改善することができる。また幹細胞は、T細胞、ナチュラルキラー細胞、マクロファージ、および樹状細胞の活性を調節することができ、感染および炎症反応を阻害することができる。さらにMSCは、標的組織に分化して修復を達成することができる。これらの影響は、miRNAおよびMEXに関連する可能性がある。
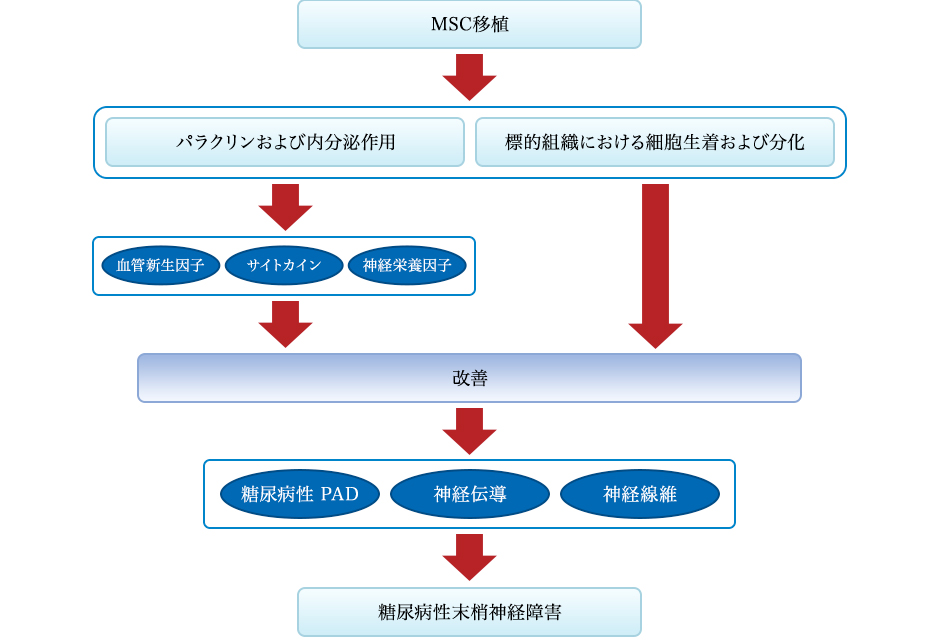
図3:糖尿病性神経障害に対するMSC移植の効果のメカニズム。二つの経路から生じる幹細胞移植によって媒介される回復効果のメカニズム:1つは血管新生因子、サイトカインおよび神経栄養因子の分泌であり、もう1つは細胞の組織構成成分への移植および分化である。
幹細胞は血管新生因子およびサイトカインの局所分泌および発現を特異的に改善することができ、糖尿病性PADおよび糖尿病自体の改善に寄与し、糖尿病性神経障害の改善につながる。神経栄養因子はまた、神経線維の機能障害および神経伝導を改善することができる。
さらに、幹細胞は標的組織に分化して修復を達成することができる。
腎不全
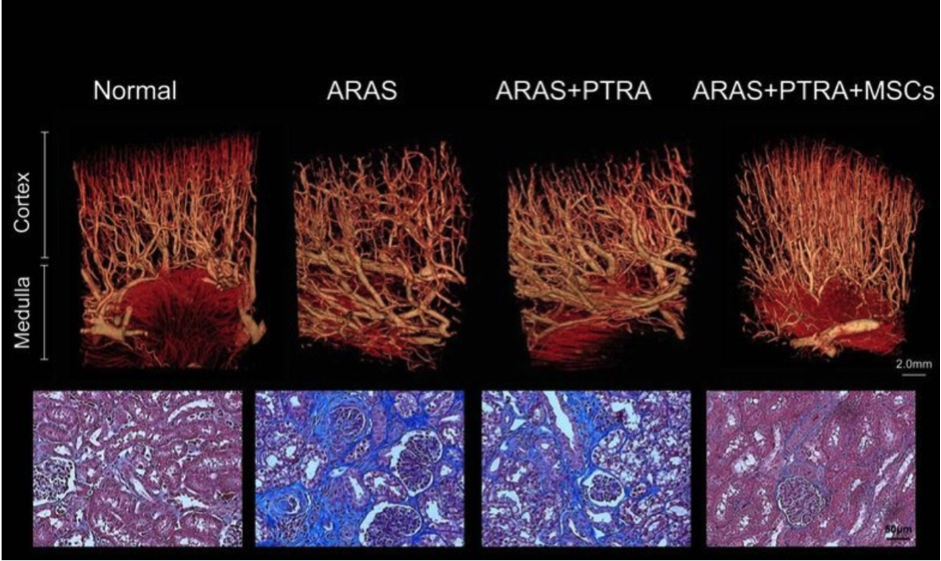
間葉系幹細胞治療を受けている動物では、狭窄 – 腎臓微小血管喪失および線維症が減少した。 上:経皮経管腎血管形成術(PTRA)を受けた、アテローム硬化性腎動脈狭窄を有するブタにおける改善された微小血管構造をとらえている、腎臓セグメントの代表的なマイクロコンピュータ断層撮影3次元画像で、4週間早く脂肪組織由来間葉系幹細胞(MSC)の副腎内注入を行った。下:ARAS + PTRA + ブタのMSC線維化の減少を示す代表的な腎トリクロム染色(×40、青色)
MSCの臨床応用例:糖尿病
幹細胞移植は、DMを有する患者にとって安全かつ有効な治療法となり得る。 この一連の試験では、T1DMについてはD34 + HSC療法で最良の治療成果が達成されたが、T1DMについてはHUCBで最悪の結果が観察された。糖尿病性ケトアシドーシスは治療効果を妨げる。
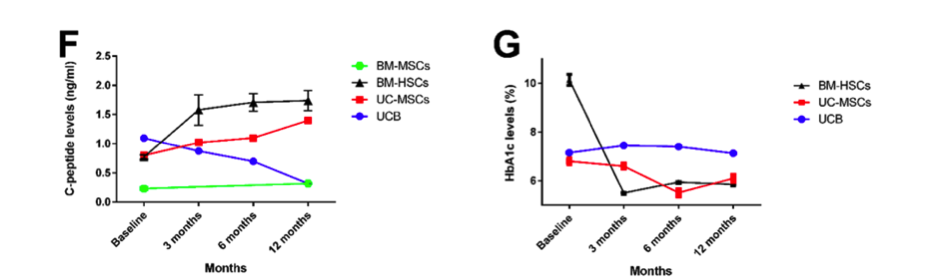
T1DM患者における幹細胞治療後のベースライン、3カ月目、6カ月目、および12カ月目におけるC-ペプチドおよびHbA1cレベルの変化を示す折れ線グラフ。 すべてのデータを平均±SEMとして表す。 **** P <0.0001
The outcome for stem cell therapy for T2DM
Stem cell therapy for type 2 DM.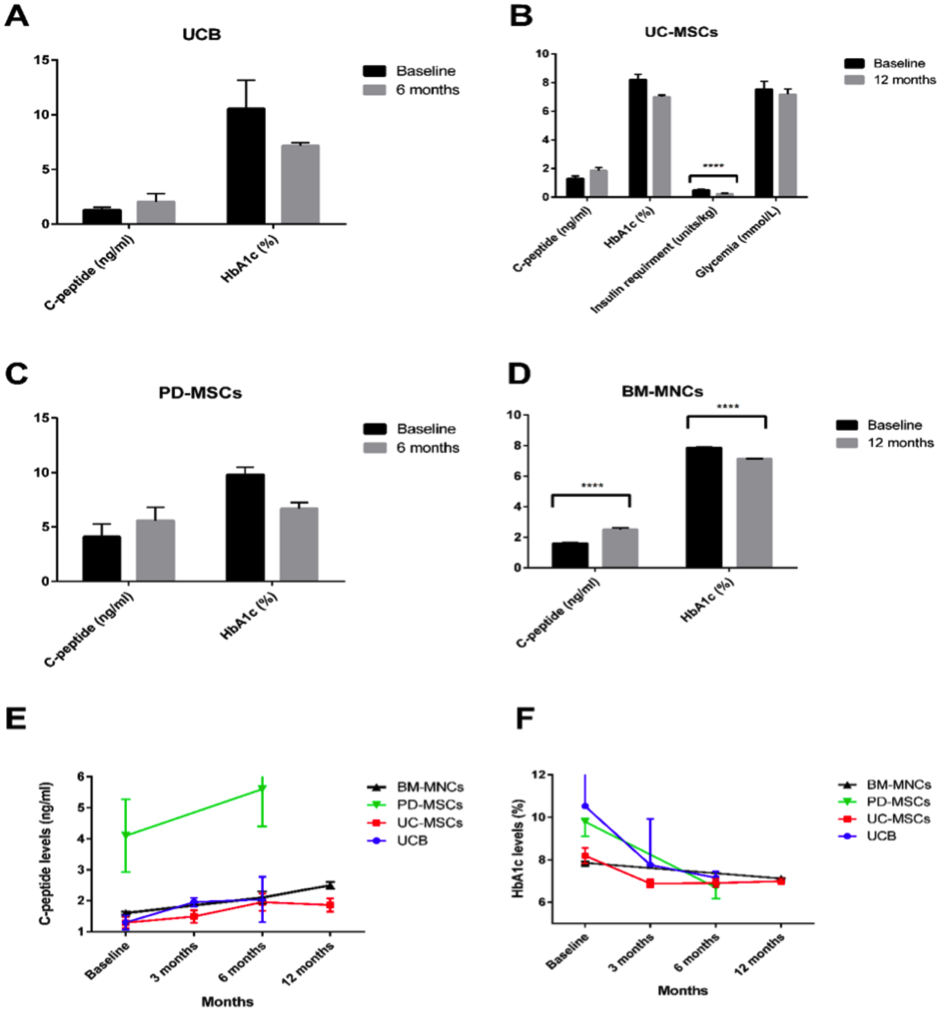
A-D)異なるタイプの幹細胞の投与後のベースライン、また12ヶ月後のC-ペプチドおよびHbA1cレベルの変化を示す棒グラフ。UC-MSCおよびPD-MSCを静脈注射した(それぞれn = 22およびn = 10)一方で、UCBおよびBM-MNCを膵臓内に注射した(n = 3およびn = 107) (E-F)T2Dにおける幹細胞治療後のベースライン、3カ月目、6カ月目、および12カ月目におけるC-ペプチドおよびHbA1cレベルの変化を示す折れ線グラフ。
Citation// PLoS One. 2016 Apr 13;11(4):e0151938. Clinical Efficacy of Stem Cell Therapy for Diabetes Mellitus: A Meta-Analysis. El-Badawy A, El-Badri N.
疾患別・毛包
Nat Commun. 2012 Apr 17;3:784. doi: 10.1038/ncomms1784.
Fully functional hair follicle regeneration through the rearrangement of stem cells and their niches.
Toyoshima KE1, Asakawa K, Ishibashi N, Toki H, Ogawa M, Hasegawa T, Irié T, Tachikawa T, Sato A, Takeda A, Tsuji T.
概要
臓器置換再生医療は、予見可能な将来において、疾患、傷害または老化によって損傷した臓器の置換を可能にすると言われている。ここで我々は、生体工学的な骨と胞子胚芽の皮内移植を介して完全に機能的な臓器再生を実証する。この胚盤葉および胚珠は、胚性皮膚由来細胞および成人幹細胞領域由来細胞でそれぞれ再構成される。バイオ工学処理された毛包は、正しい構造を発達させ、表皮、後肢筋肉および神経線維のような周囲の宿主組織との適切な接続を形成する。バイオ工学的に生成された毛包は、毛包幹細胞およびそれらのニッチの再編成を介して回復した毛周期および毛頭形成をも示す。従ってこの研究は、成体組織由来毛包幹細胞の生物工学的臓器置換療法としての可能性を明らかにする。
 .
.
(a)バイオ工学処理された毛包胚の作製および移植に使用される方法の概略図。(b)ナイロンの糸(矢頭)を用いて、臓器胚芽法を用いて再構成された、マウスの胚の背部皮膚、組織、解離した単細胞およびバイオ工学による毛包胚の位相差画像。縮尺、200μm。
(c) 成体マウスからの単離した触毛の組織学的分析。巨視的およびH&E染色の触毛が左の2つのパネルに示されている。マクロ形態学的観察(左)およびH&E染色(右)による破線(赤色)は、バルジおよびSB領域の界面を示す。左パネルのボックス領域は、バルジを示すためにH&E染色され、SB領域は右パネルのより高い拡大図で示される。バルジ領域は、抗CD49f(赤、左)および抗CD34(赤、中央)抗体およびHoechst
33258色素(青)で免疫染色された。高倍率のH&Eにおける黒い破線は、毛包の上皮の界面を示す。IF、漏斗; RW、環状体;毛包の半分。縮尺、100μm。(d)
触毛のバルブ領域およびDP細胞の初期培養の組織学的およびALP分析。毛球(左2匹)および培養したDP細胞(右2匹)をALPの酵素染色により分析した。赤い点線はAuberの線を示しています。縮尺「、100μm。
(e) 上皮間組織連結プラスチック装置(ガイド付き)によって仲介される、噴出および成長プロセス中のバイオ工学処理された毛の縦断面。対応するものは、(ガイドなしで)皮内移植の14日後にバイオ工学的に生成された毛胞を伴う嚢胞形成として示される。移植後0日、3日および14日に、バイオ工学的に生成された毛胞のH&E染色(上)および蛍光顕微鏡(下)。縮尺、100μm。
(f) 0日目の移植直後(左)、3日目(中央)の創傷の治癒、14日目と37日目(右)の毛幹の噴出、および成長を含む、バイオ工学的に生成された胸部(上)および脾臓(下)の発育および成長の間の生育した毛髪のマクロ形態学的観察。
縮尺、1.0mm。
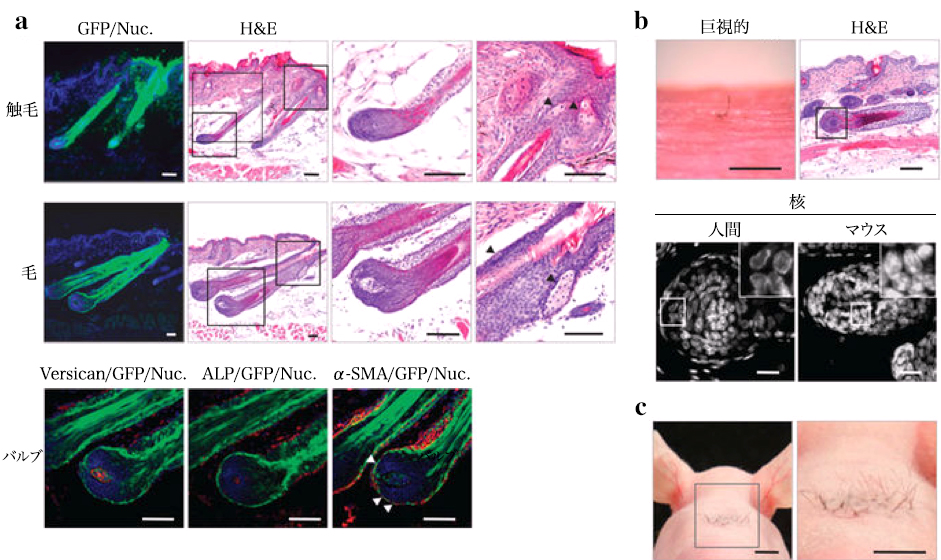
(a) バイオ工学的な毛(上部)および触毛(中央)小胞の組織学的および免疫組織化学的分析。低倍率のH&Eパネルのボックス領域は、右側のパネルでより高い倍率で示されています。矢印は皮脂腺を示す。縮尺、100μm。バイオ工学処理された毛包の毛球は、抗
– バーシカン(左下)およびα-SMA(矢頭、右下)抗体で免疫染色され、ALPについても酵素的に染色された。(下中央)縮尺、50μm。 (b)
バイオ処理された毛包胚の移植によって産生された生物工学によるヒトの毛髪は、バルジ由来の上皮細胞およびヒトの頭皮毛包の無傷のDPによって再構成された。移植後21日目に、バイオ工学によるヒトの毛髪を撮影し(顕微鏡検査)、H&E染色によって分析した。核形態学的特徴(右パネル)に従って、バイオ工学処理された毛包の種同定が分析された。挿入図の囲まれた領域は、高い倍率で示される。縮尺、顕微鏡500μm、H&E100μm、核染色20μm。(c)
バイオ工学処理された毛胞病原体の高密度皮内移植。マウスの子宮頸部皮膚に合計28の独立したバイオ工学的毛包胚芽を移植し、移植後21日目に高密度の毛髪成長を示した。縮尺、5mm。
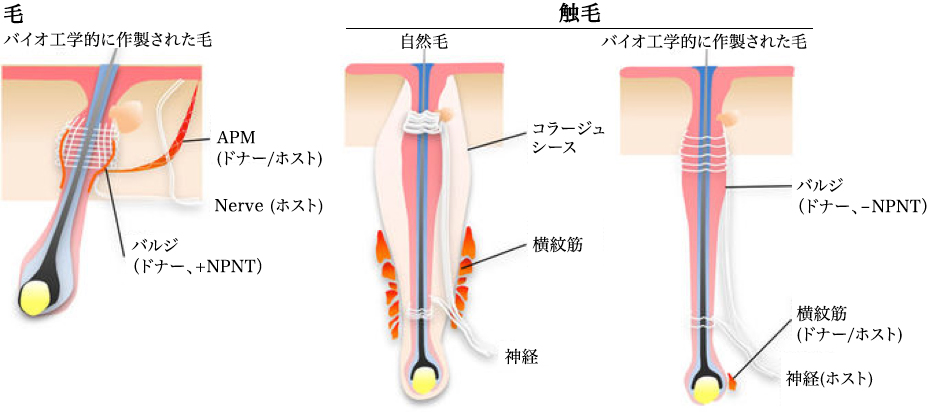
バイオ工学的に産生された毛および触毛は、宿主細胞またはドナー細胞に由来する神経繊維、牽引筋および線条筋などの他の組織と連結した。バイオ工学的に作製された毛は、自然の塊状物と同様にNPNTを発現するバルジ領域の再生の結果として、平滑筋に結合した。NPNT発現も平滑筋結合も、バイオ工学的な毛のバルジ領域では検出されなかった。
引用/ Fully functional hair follicle regeneration through the rearrangement of stem cells and their niches. Koh-ei Toyoshima, Kyosuke Asakawa, Naoko Ishibashi, Hiroshi Toki, Miho Ogawa, Tomoko Hasegawa, Tarou Irié, Tetsuhiko Tachikawa, Akio Sato, Akira Takeda & Takashi Tsuji. Nature Communications 3, Article number: 784 (2012)
doi:10.1038/ncomms1784
他疾患・パーキンソン
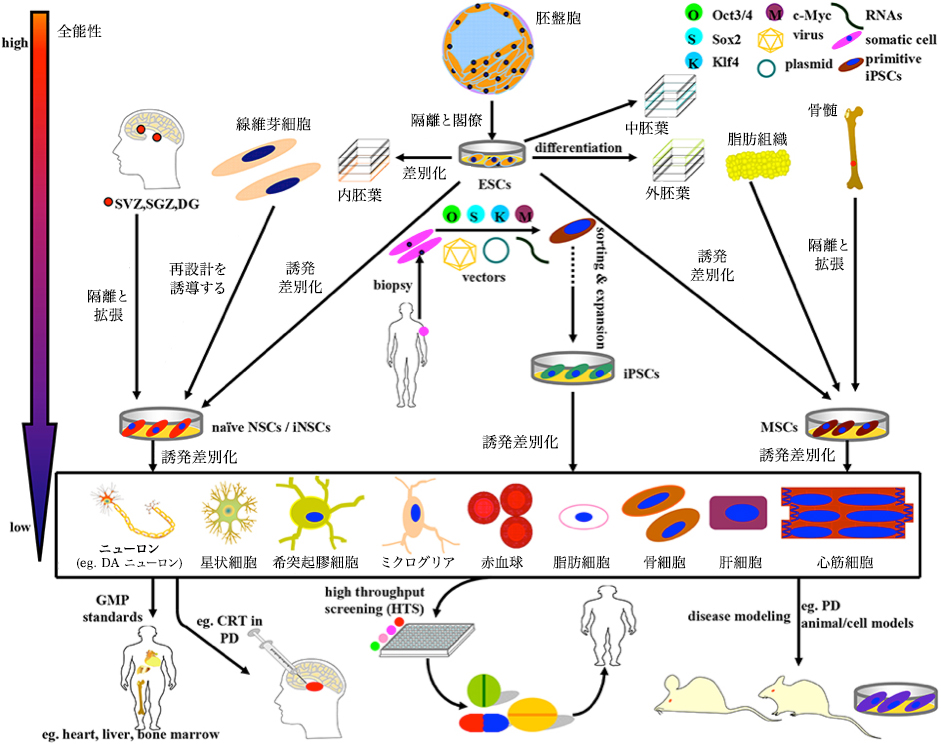
PD研究および治療で現在利用可能な幹細胞の誘導、分化および適用の概略図。上記の幹細胞は、ESC、NSC、MSC、およびiPSCの4つのカテゴリーに分けることができ、徐々に減少する分化全能性を伴う。
(1) 主に胚盤胞内部塊に由来するESCは、通常の状況下で同時に内胚葉、中胚葉および外胚葉に分化することができる。 場合によっては、ESCもNSCおよびMSCに分化するように誘導することができる。
(2) 特定の脳のニッチから直接単離した、または線維芽細胞から再プログラムしたNSCは、ニューロンおよびほぼすべての神経膠細胞への神経系統の分化を行うことができる。(3)
MSCは、主に間葉組織に由来し、中胚葉起源のほとんどすべての細胞に分化することができる。顕著なことに、MSCは誘導プロトコルの特定の組み合わせの下でもDAニューロンに分化するように誘導することができる。(4)
OSKM(Oct3 / 4、Sox2、Klf4、およびc-Myc)を導入することにより、成人のヒト体細胞(線維芽細胞など)から再分化させることができるiPSCsは、多系譜分化能を有する有望な幹細胞源である。GMP標準に基づいて、上記の幹細胞および最終分化細胞を、疾患モデル、薬物スクリーニング、およびCRTの実施に適用するために、さらに選別し、精製し、そして拡大することができる。例えば、ESC、MSC、NSC、およびDAニューロンは、以下で使用される。(i)PDモデルの準備(ii)潜在的な薬物スクリーニング;(iii)PDのCRT治療Front.
Aging Neurosci., 31 May 2016. A Compendium of Preparation and Application
of Stem Cells in Parkinson’s Disease: Current Status and Future Prospects.
Yan Shen, Jinsha Huang